氷に塩をかけるとマイナス20度まで温度が下がる理由:水と塩の不思議な関係
手作りアイスクリームを作る器具に、氷に塩をかけて冷やすものがあるのをご存知でしょうか。
氷に塩をかけるのは、氷が入っている部分の温度0度より下げるためですが、なぜ氷に塩をかけると温度が下がるのでしょうか?

先ず、暖かい部屋に大きな氷を出したところを想像してみてください。大きな氷の塊なら部屋の温度が下がり、氷は時間経過に連れて融け、 周囲は融けた水で溢れてしまうことは理解できると思います。
融解熱とは
なぜ部屋の温度が下がるのでしょうか?
考えられることは一つ、氷が熱エネルギーを吸い取って、水になったということです。
では、なぜ、氷が水になるときにエネルギーを必要とするのでしょうか?
氷は水素原子2個と酸素原子1個で構成された水分子が周囲の水分子と強固に結びついたものです。そのために氷は自由な形にならないのです。
対して液体の水の場合は、水分子同士の結びつきが少し弱くなり、水分子は自由に動けるようになるために複雑な形をした容器にでも隙間なく入ることが出来るようになります。
水分子が持っているエネルギーの大きさを水と氷の状態で考えると、 私たち人では運動すれば動かないで寝ているときよりエネルギーを必要としますから、動けない水分子よりも動ける水分子の方がエネルギーをたくさん持っていると直感的に理解出来ると思います。エネルギーを持っていなければ動けないので、人や動物は食べることによって他からエネルギーを得ますが、水分子は接している分子から熱伝導としてエネルギーを得ます。
熱は温度が高い所から低い所に移動しようとするのが自然の摂理なので、空気中に置いた氷は接している空気が温かければ空気からエネルギーを得て水分子は少し自由に動けるようになって液体に変わります。この状態の変化に必要な熱量を融解熱 と言います。
氷に接している側から見れば、固体の氷から液体の水になるときにエネルギーを奪われるので温度が下がります。
氷に掛ける塩の役割
氷に塩をかけると、融けていた水に塩が溶けます。 塩が水に溶けるというのは、塩を構成している塩素とナトリウムの結び付きが切れて、塩素がマイナスの電気を帯び、 ナトリウムがプラスの電気帯びてイオン化し、下イメージ図のようにその周囲に水分子を電気的に結合させて安定することです。 このとき、エネルギーを必要とするので周囲から熱エネルギーを奪いますから、周囲の温度が下がります。
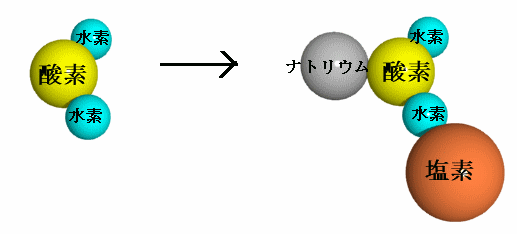
もうひとつ大事なことは、塩水を凍らせるには、水分子から塩素やナトリウムのイオンを離さなければならないので、 そのためのエネルギーを外部から必要とするので水が凍る0度では凍らないということです。
まとめると、氷に塩をかけると、 氷が水になるときに周囲から熱を奪う融解熱 と、塩が水に溶けるときに周囲から奪う溶解熱
の相乗効果で温度が下がり、温度が下がっても塩水のために周囲の水が再び凍ることがないので反応が止まることがなく温度が下がるのです。
質量で、氷の3分の1の塩を振り掛けると、零下20度まで下がるそうです。 冷凍庫が壊れると氷よりアイスクリームの方が先に溶け出すことで解るように、アイスクリーム作りには氷作りより低温が必要なので凍りに塩を掛けて低温を作り出す器具が作られたのでしょう。